Le intolleranze alimentari sono da sempre un’entità molto discussa. Esistono diversi tipi di test che promettono di diagnosticarle ma… esistono veramente? Vediamo di capirci qualcosa insieme partendo da quanto riportato dall’Istituto Superiore di Sanità, anche se vi premetto che su alcune cose non sono d’accordo.
Intolleranze alimentari e Allergie: quale è la differenza?
Quando mangiamo una qualsiasi cosa possiamo andare incontro ad una “reazione avversa ad un alimento” (RAA). La RAA può essere determinata da uno qualsiasi dei componenti dell’alimento, siano essi naturali o aggiunti (per esempio, gli additivi, i conservanti, i coloranti). Non rientra in questa definizione l’ingestione di alimenti contaminati da batteri, virus o parassiti, che rientrano nelle tossinfezioni alimentari.
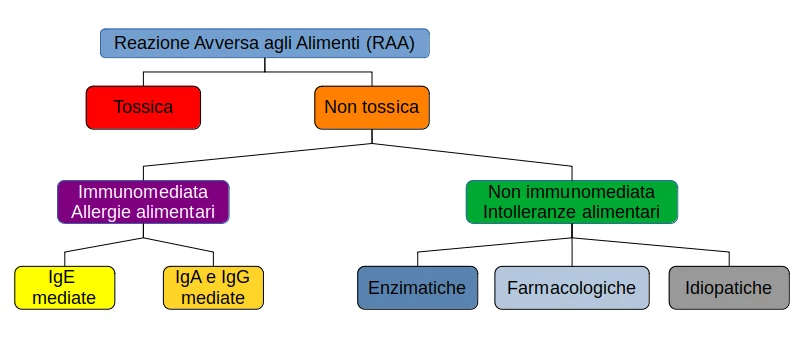
La RAA può essere di tipo Tossico, quando l’alimento contiene una sostanza tossica in grado di bloccare enzimi chiave del nostro organismo, oppure Non tossico, la stragrande maggioranza dei casi.


Le reazioni di tipo Non Tossico possono essere Mediate dal sistema immunitario e sono quelle che si definiscono Allergie vere e proprie e poi ci sono quelle Non mediate dal sistema immunitario e sono quelle che si definiscono Intolleranze.
Le allergie, nella stragrande maggioranza dei casi, sono mediate dagli anticorpi di classe IgE, ma possono essere mediate anche da anticorpi di tipo IgA e IgG; le intolleranze posso essere:
- Enzimatiche – mancano o non funzionano bene particolari enzimi;
- Farmacologiche – determinate da sostanze che hanno un’azione farmacologica come le ammine vasoattive (istamina, tiramina e feniletilammina);
- Idiopatiche – non si conosce ancora il meccanismo con cui agiscono.
Le allergie Ig-E mediate
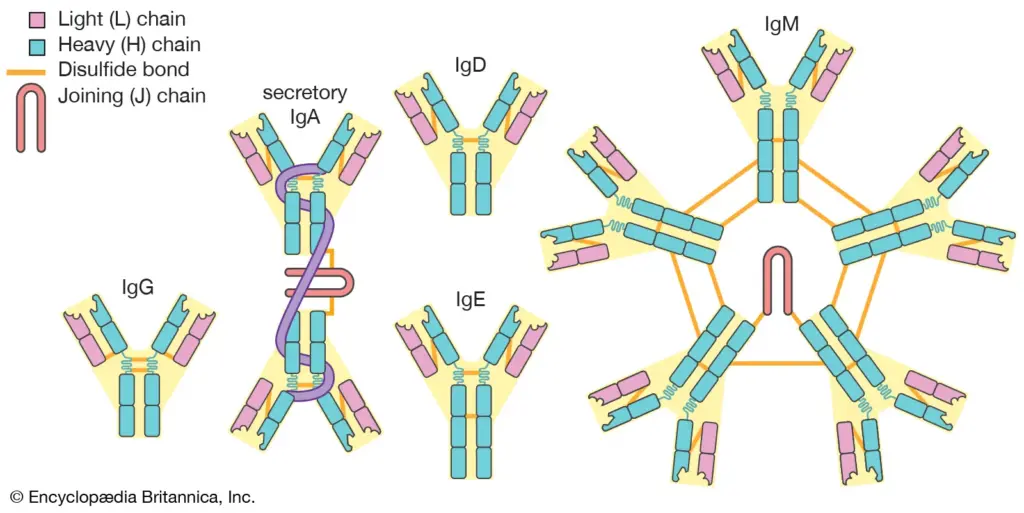
Gli anticorpi della classe IgE hanno una particolarità: hanno un “dominio” che gli consente di agganciarsi ed “armare” i mastociti, un sottotipo di globuli bianchi.
Quando le IgE legano l’antigene, i mastociti “degranulano”, liberando l’istamina che è la responsabile di tutta la sintomatologia allergica.
Esistono vari test per determinare a cosa si è allergici, ma allo stato attuale, esistono test di tipo molecolare che sono in grado di testare, contemporaneamente, circa 300 allergeni. Quali sono i principali antigeni allergenici? Vediamoli.
PR-10
Possiamo identificare due tipi di meccanismi:
- Inalazione
Bet-v-1, il principale allergene del polline di betulla, rappresenta il prototipo di tutti gli allergeni PR-10 ed è anche il sensibilizzatore primario PR-10 nelle aree endemiche di betulla. La presenza di allergeni PR-10 in altri pollini di piante della specie delle Fagali spiega la pronunciata cross-reattività al polline di ontano, nocciolo, faggio, quercia e carpino. - Assunzione orale
Gli allergeni PR-10 in frutta, noci, legumi e verdure possono scatenare allergie alimentari associate, di solito limitate a una sindrome di allergia orale. In rari casi, può anche portare a gravi reazioni allergiche. Gli allergeni PR-10 sono sensibili al calore e alla digestione.
Gli allergeni PR-10 mostrano un alto tasso di cross-reattività.
Profilina
A seconda della popolazione, fino al 50% dei soggetti allergici ai pollini è sensibilizzato alla profilina. La sensibilizzazione a profiline può portare a sintomi respiratori. Fino al 50% degli individui sensibilizzati alle profiline può sviluppare un’allergia alimentare associata, in genere limitata a una sindrome da allergia orale. Pomodoro crudo, melone, anguria e agrumi sono in genere associati a un’allergia alimentare da profilina. Le profiline sono sensibili al calore e alla digestione.
La Profilina mostra un alto tasso di cross-reattività.
Ole-e1
Ole-e1, il principale allergene del polline di oliva ed è anche il sensibilizzatore primario nelle regioni endemiche degli ulivi. Altri membri della famiglia Ole-e1 sono stati identificati nel polline di altre piante della famiglia degli ulivi (cenere, lillà, ligustro). Ci sono anche altri membri della famiglia degli Ole-e1 nell’erba e nel polline dell’erba.
Gli allergeni della famiglia Ole-e1 mostrano un alto grado di cross-reattività all’interno della famiglia botanica.
Proteine di trasporto dei lipidi (nsLTP)
Le nsLTP sono gli allergeni alimentari vegetali maggiormente presenti nell’Europa meridionale. Le reazioni cliniche indotte da nsLTP possono essere gravi, specialmente dove non c’è alcun legame con la pollinosi di betulla. Pru-p3, il principale allergene della pesca, svolge un ruolo precursore nel sensibilizzare contro altri nsLTP. Le nsLTP allergologicamente rilevanti si trovano non solo nella famiglia delle Rosacee (incluse pomacee e drupacee), ma anche in noci, legumi e cereali (grano, mais o riso). Le nsLTPs sono stabili al calore e alla digestione e mostrano un alto grado di cross-reattività all’interno della famiglia botanica.
Proteine di deposito (Albumina 2S, globuline 7/8S, globuline 11S)
Le proteine di deposito sono i principali allergeni nei legumi (ad es., Arachidi o semi di soia), negli alberi da noci (ad es. nocciole) e altri semi (ad esempio grano saraceno, grano o senape). Esse sono la causa principale di gravi reazioni allergiche, inclusa l’anafilassi; sono stabili al calore e alla digestione ma mostrano un limitato tasso di cross-reattività.
Tropomiosine
La sensibilizzazione alle tropomiosine può essere causata dall’ingestione di alimenti ittici, dall’inalazione di componenti di acari o di scarafaggi o da infezioni parassitarie (ad es. Anisakis simplex). Le Tropomiosine sono stabili al calore e alla digestione, mostrano un tasso molto elevato di cross-reattività e possono scatenare diversi tipi di reazioni allergiche, compresa l’anafilassi.
Arginina Chinasi
La sensibilizzazione alle Arginina Chinasi può essere causata dal consumo di frutti di mare e dall’inalazione di componenti di frutti di mare, acari o scarafaggi. Le Arginina Chinasi hanno un tasso di cross-reattività molto elevato e sono instabili al calore e alla digestione.
Uteroglobine
Le Uteroglobine si formano nelle ghiandole salivari e nella pelle di alcuni animali da pelliccia. Nei bambini con asma allergico da gatto, sono stati rilevati livelli più elevati di IgE verso le Uteroglobine. Le Uteroglobine hanno un limitato tasso di cross-reattività.
Lipocaline
Le Lipocaline, anch’esse prodotte da animali da pelliccia (ma anche dallo scarafaggio), sono trasportate per via aerea e facilmente diffuse negli ambienti chiusi. Costituiscono un fattore di rischio per sintomi respiratori e asma. L’impatto delle sensibilizzazioni individuali alla lipocalina sulla gravità dei sintomi è ancora sconosciuta e mostrano un limitato tasso di cross-reattività.
NPC2
Membri della famiglia NPC2 sono presenti negli acari della polvere domestica e negli acari delle derrate. La cross-reattività tra Der-f2 e Der-p2 è piuttosto estesa. Gli allergeni NPC2 da acari delle derrate hanno un limitato grado di cross-reattività con gli acari della polvere domestica.
Le allergie non mediate da IgE
In questa categoria rientra la Celiachia (classificata, ahimè, come Intolleranza al glutine dall’Istituto Superiore di Sanità).
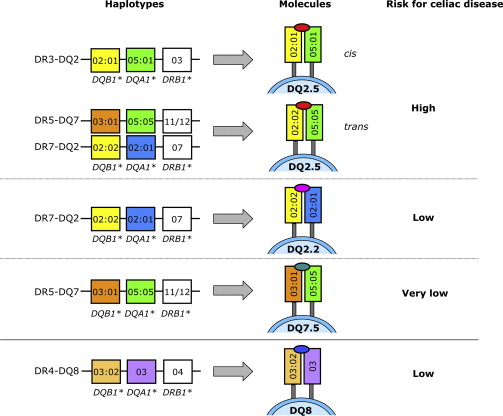
In soggetti geneticamente predisposti, con un particolare assetto dei geni HLA-DQB1, HLA-DQA1 e HLA-DRB1, evidenziabile con un test di biologia molecolare, possono produrre auto-anticorpi di classe IgA e IgG diretti contro antigeni tissutali umani, scatenando una risposta di tipo auto-immune. Vanno titolati entrambe le classi perché i bambini possono avere un deficit secretorio di IgA.
Quali anticorpi dosare?
Anticorpi anti Endomisio (EMA) – IgA
I primi ad essere individuati. Hanno una sensibilità bassina e sono andati in disuso.
Anticorpi anti Gliadina deamidata (DGP) – IgA e IgG
Test di nuova generazione, con una sensibilità del 75% ed una specificità del 94%
Anticorpi anti Transglutaminasi (tTG) – IgA e IgG
Gli anticorpi che fanno testo, avendo sensibilità del 94% ed una specificità del 98%
Le intolleranze alimentari
E finalmente ci siamo arrivati a queste benedette intolleranze alimentari. Se avete letto bene i paragrafi precedenti, avete visto che molto spesso trattasi di vere e proprie allergie, più che di Intolleranze. Vediamo ora di capire quali sono le vere intolleranze alimentari.
Intolleranze alimentari geneticamente determinate
In questa classe rientra la maggior parte delle intolleranze alimentari note. Un enzima assente o mal funzionante causa l’accumulo di un metabolita che genera la reazione avversa.
Intolleranza alle fave – Favismo
La carenza di Glucosio-6-Fosfato-Deidrogenasi (G6PD) è il deficit enzimatico umano più comune, probabilmente perché questa deficienza enzimatica conferisce resistenza alla malaria.
Il favismo è la manifestazione clinica della carenza di G6PD ed è conosciuta sin dall’antichità: il famoso filosofo e matematico Pitagora impose ai suoi discepoli il divieto di cibarsi di fave.
Ma cosa accade? Nelle fave sono contenute la vicina e la convicina, due sostanze che, nei soggetti fabici, inducono una crisi emolitica, ossia la rottura dei globuli rossi, la liberazione dell’emoglobina con apertura dell’anello eme in bilirubina e conseguente anemia acuta. La bilirubina è la responsabile della colorazione gialla della cute e delle sclere dei soggetti con crisi emolitica in atto (ittero).
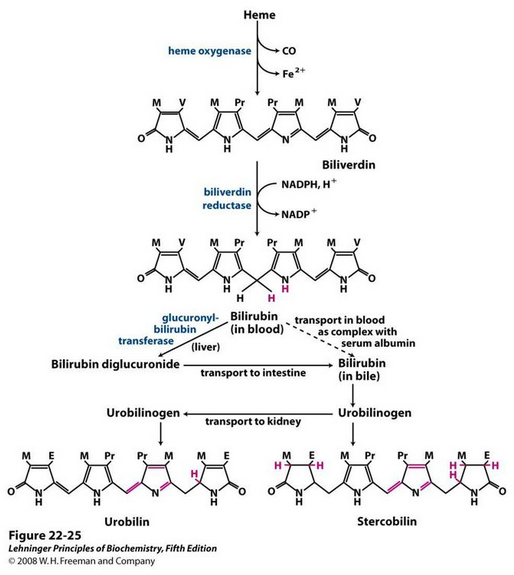
Solo le fave contengono la vicina e la convicina e tutta una serie di miti su altri legumi, tipo: piselli, fagioli, ceci, lenticchie, lupini o mirtilli, vino rosso, acqua tonica sono stati ampiamente smentiti (qui un’intervista in proposito al mitico prof. Lucio Luzzatto). Tuttavia, il soggetto fabico può andare incontro a crisi emolitiche causate da farmaci come la primachina o l’acido acetil-salicilico. L’elenco completo dei farmaci da evitare è messo a punto dall’Istituto Superiore di Sanità e lo trovate qui.
Intolleranze alimentari – glicidi
Intolleranza al lattosio
Questa è l’intolleranza più nota ed è dovuta alla mancanza della proteina Lattasi codificata dal gene LCT. Ne abbiamo già parlato nel blog (trovi l’articolo qui) e, oltre al test genetico, è possibile diagnosticarla con un Breath test.
Intolleranza al fruttosio (fruttosemia)
La fruttosemia è una intolleranza grave, letale se non curata immediatamente, ed è dovuta a mutazioni nel gene che codifica per l’Aldolasi B (ALDOB), un enzima chiave della glicolisi. L’accumulo epatico di fruttosio blocca la liberazione di glicogeno e questo causa delle ipoglicemie severe quando si assume questo zucchero.
Intolleranza al galattosio (galattosemia)
Il lattosio è un disaccaride che deve essere scisso in glucosio e galattosio. Il galattosio, per essere utilizzato, deve essere trasformato in glucosio.
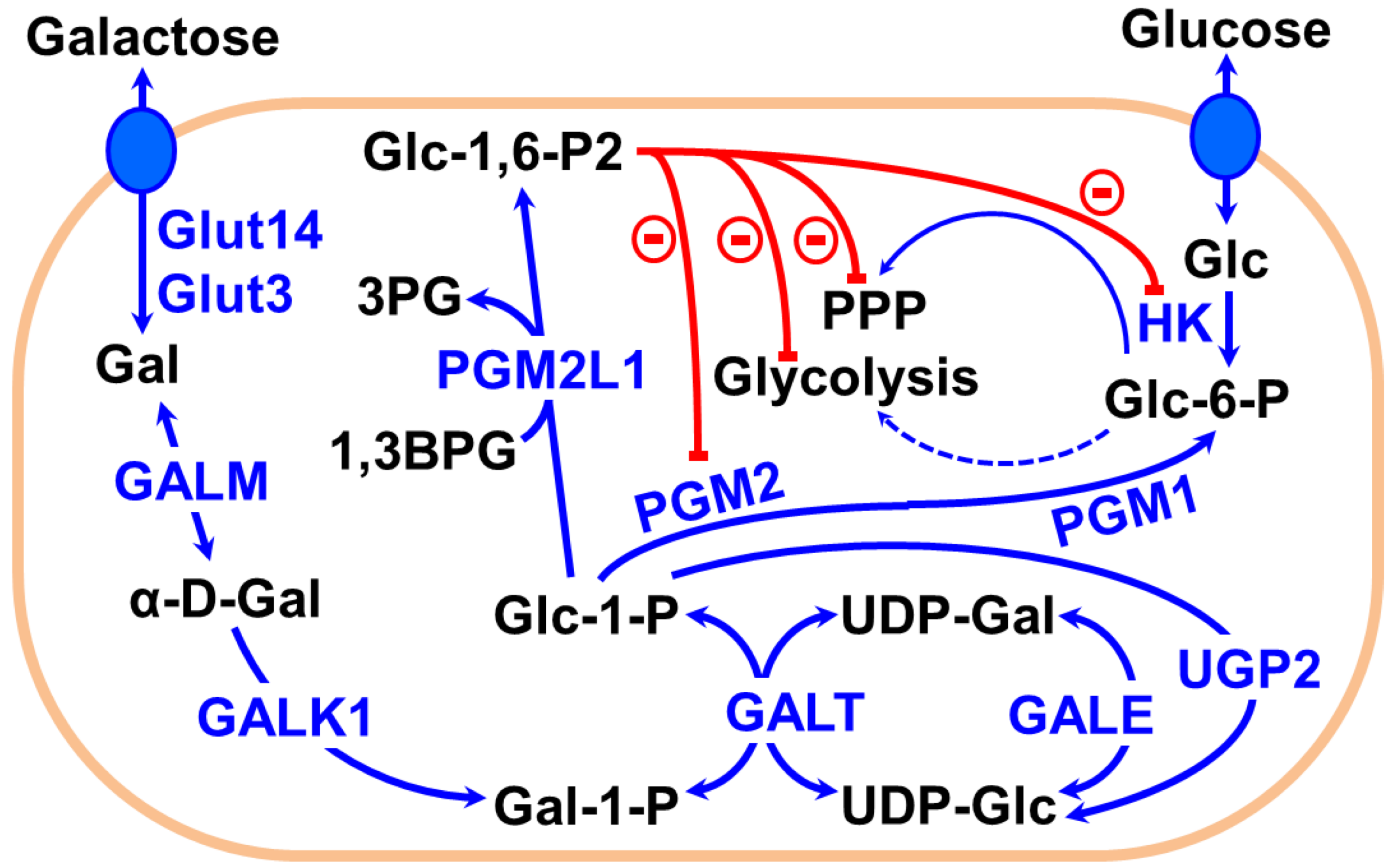
Una qualsiasi mutazione che induca il malfunzionamento di una delle proteine GALT, GALK1, GALK2, GALE, GALM blocca questa via metabolica. La galattosemia è una malattia rara ed i soggetti che ne sono affetti non possono eseguire il breath test al lattulosio, così come abbiamo anche scritto nel precedente blog dedicato.
Malassorbimento Glucosio-Galattosio
La sindrome da malassorbimento di glucosio-galattosio è una condizione rara caratterizzata dalla comparsa, in epoca neonatale, di grave diarrea acquosa e acida. Come per la fruttosemia, tale intolleranza può risultare fatale se i due monosaccaridi non vengono rimossi dalla dieta. L’etiologia di questa patologia autosomica recessiva, è da ascriversi a mutazioni nel gene SLC5A1, che codifica per il trasportatore sodio dipendente del glucosio e galattosio.
Deficit Saccarasi-Isomaltasi
Il deficit congenito di saccarasi-isomaltasi (CSID) è una rara malattia genetica dovuta a mutazioni nel complesso enzimatico della Saccarasi-Isomaltasi (SI), causando ritenzione dei disaccaridi nel lume intestinale e generando diarrea osmotica e dolore addominale.
Deficit di Trealasi
Per completezza, citiamo anche il deficit di trealasi dovuto a mutazioni nel gene TREH, che non consente di scindere il trealosio, un disaccaride presente nei funghi, causando l’intolleranza verso questi ultimi.
Intolleranze alimentari – amminoacidi
Sono tutte rare e particolarmente gravi, per cui ci soffermiamo unicamente su quella più nota e trattata.
Fenilchetonuria
In questo caso, il gene che non funziona è quello che codifica per la Fenilalanina Idrossilasi (PAH). L’amminoacido Fenilalanina non viene convertito in Tirosina, si accumula e viene convertito in acido Fenilpiruvico e acido Fenilacetico, altamente tossici per il cervello. I soggetti affetti da fenilchetonuria devono avere un regime alimentare a basso contenuto di fenilalanina. Proprio per questo, i soggetti affetti da iperfenilalaninemia non devono assumere cibi dolcificati con l’aspartame (L-aspartil-L-fenilalanina metilestere) e non basta indicare la sua presenza sulle etichette, bisogna apporre anche la frase “Contiene una fonte di fenilalanina“.

Intolleranze alimentari – lipidi
In questa categoria rientrano tutte le displipidemie più o meno gravi: dalla ipercolesterolemia familiare dovuta al deficit del recettore delle LDL o a deficit delle proteine di trasporto, come Lp(a), ApoA1, ApoB (proteine di cui chiediamo il dosaggio nel nostro referto cardiometabolico) o a deficit di proteine che hanno il compito di tagliare i lipidi, le lipasi.
Intolleranza al sale
Questo argomento è estremamente dibattuto nella comunità scientifica visto che la “sensibilità” o intolleranza al sale, il cloruro di sodio, colpisce il 50% degli ipertesi e il 25% dei normotesi.
La risposta della Pressione Arteriosa all’assunzione di sale non è uniforme tra gli individui. Come definito dall’ACC/AHA, la sensibilità al sale è “un tratto fisiologico presente nei roditori e in altri mammiferi, compreso l’uomo, in cui la pressione arteriosa di alcuni membri della popolazione mostra cambiamenti paralleli ai cambiamenti nell’assunzione di sale”.
In questi pazienti, il carico acuto di sale provoca maggiori picchi di pressione arteriosa e la privazione di sale provoca maggiori cali di pressione rispetto agli individui resistenti al sale. Per chi volesse approfondire, qui trova una review fatta molto bene. Proprio perché la risposta è molto eterogenea, la sensibilità al sale è un tratto poligenico; molte varianti geniche in geni diversi possono contribuire, in maniera più o meno sinergica, a determinare questa condizione. Il gene sicuramente più testato nei laboratori è quello dell’Enzima di Conversione dell’Angiotensinogeno (ACE), ma ce ne sono tanti altri, che potete trovare in quest’altra review.
Intolleranze alimentari da deficit enzimatico o farmacologiche?
L’Istituto Superiore di Sanità ci informa che le sensibilità farmacologiche emergono in individui che manifestano una sensibilità particolare a specifiche sostanze contenute in determinati alimenti. In alcuni scenari, inoltre, la risposta può essere attribuita a determinati additivi introdotti nei cibi. Non è ancora chiaro se, in questo contesto, si tratti di intolleranza o allergia: al momento non esistono prove che supportino un’origine immunologica della reazione, ma le manifestazioni variano così ampiamente che non è possibile escludere la possibilità di un’interazione tra meccanismi biochimici e quelli mediati immunologicamente.
Per molte delle sostanze riportate nelle Tabelle dell’ISS è noto il deficit enzimatico e quindi non sono intolleranze farmacologiche.
Intolleranza all’istamina
Questa intolleranza è dovuta al mancato metabolismo dell’istamina, introdotta col cibo o formata dai batteri intestinali, dovuta al malfunzionamento della proteina DiAmminoOssidasi codificata dal gene AOC1. L’istamina si accumula, viene assorbita dall’intestino e viene mandata in circolo, scatenando una sintomatologia da reazione pseudo-allergica (non è stata prodotta dalla degranulazione dei mastociti armati di IgE).
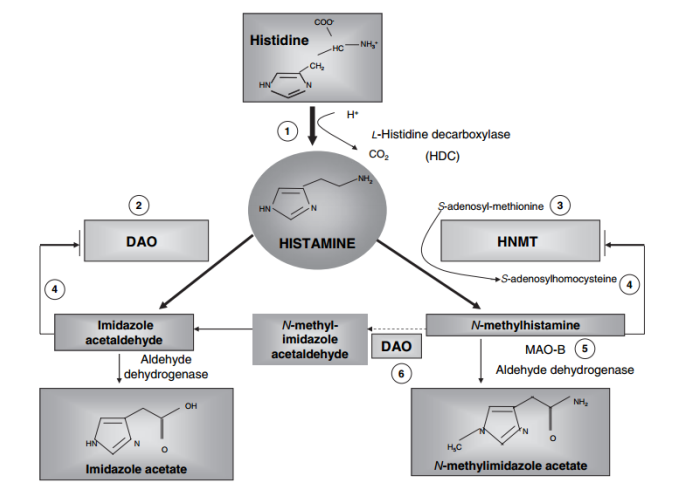
Le mutazioni del gene AOC1 rs2052129 e rs2268999 inducono una ridotta sintesi di mRNA; la mutazione rs1049742 induce una ridotta attività catalitica dell’enzima; la mutazione rs10156191 induce una ridotta sintesi di mRNA ed una ridotta attività catalitica dell’enzima. La presenza di una mutazione in omozigosi o di due o più mutazioni in eterozigosi composita inducono intolleranza all’istamina e una ipersensibilità ai FANS (farmaci antiinfiammatori non steroidei).
Inoltre, ci possono essere farmaci che inibiscono DAO o aumentano il rilascio di istamina
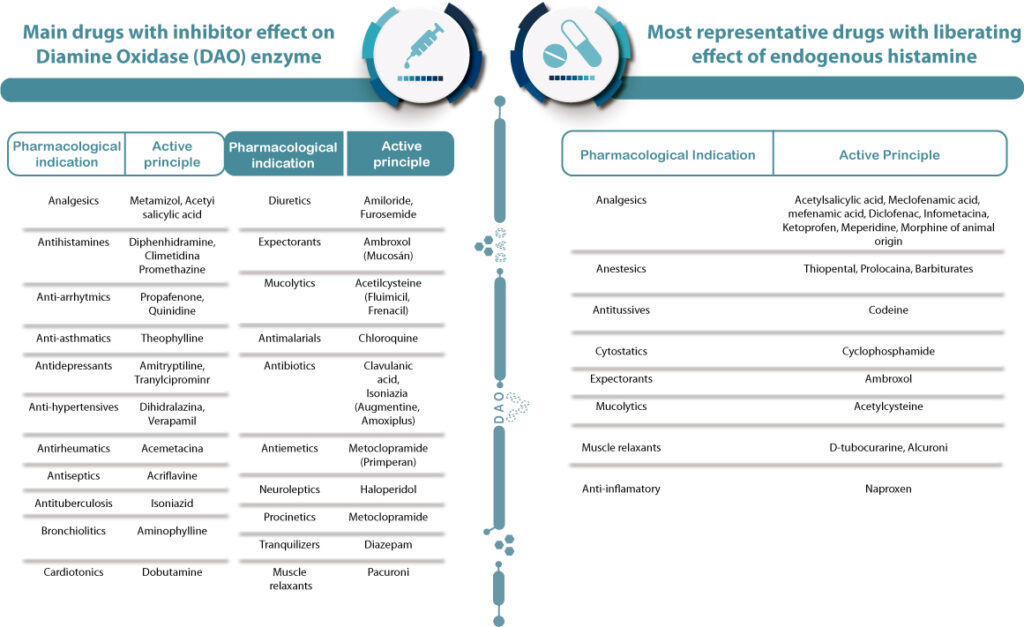
Poiché l’istamina rimane non degradata nelle feci, nel nostro laboratorio è possibile dosarla o da sola o insieme a calprotectina e zonulina.
Intolleranza all’etanolo
L’etanolo è una molecola particolarmente tossica per noi e quindi il suo metabolismo è ridondante: può prendere la via dell’alcool deidrogenasi, quella del sistema microsomiale e, infine, quella della catalasi. Tutte e tre porteranno l’etanolo ad acetaldeide (che è la molecola responsabile del mal di testa da sbronza) che l’aldeide deidrogenasi converte in acetato.
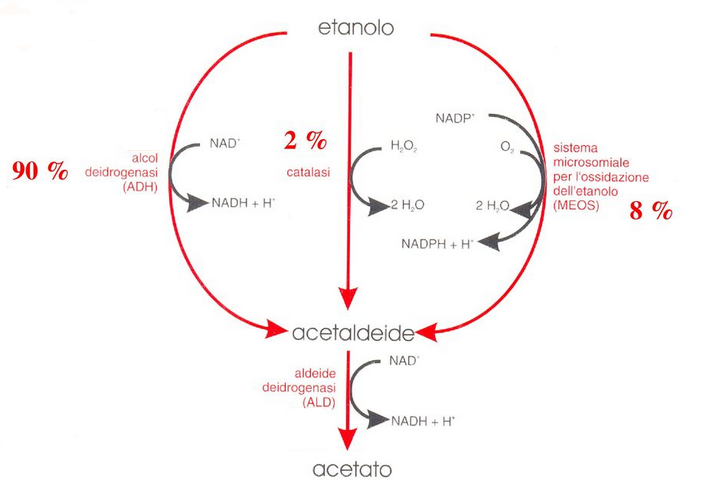
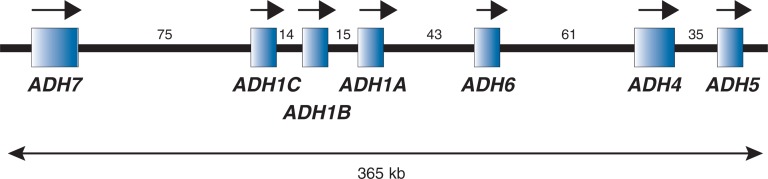
Anche l’intolleranza all’etanolo è geneticamente determinata. Può dipendere dal deficit dell’alcool deidrogenasi, che è espressa in diverse “varianti”: infatti si tratta di una famiglia genica (ADH1A, ADH1B, ADH1C, ADH4, ADH5, ADH6, ADH7).
Anche l’aldeide deidrogenasi esiste in due forme, una citosolica e una mitocondriale, e le due forme sono espresse da due geni diversi su due cromosomi diversi (quindi niente cluster). Anche mutazioni nei geni ALDH1 e ALDH2 possono dare intolleranza all’etanolo per accumulo di acetaldeide. Per approfondimenti, cliccare qui.
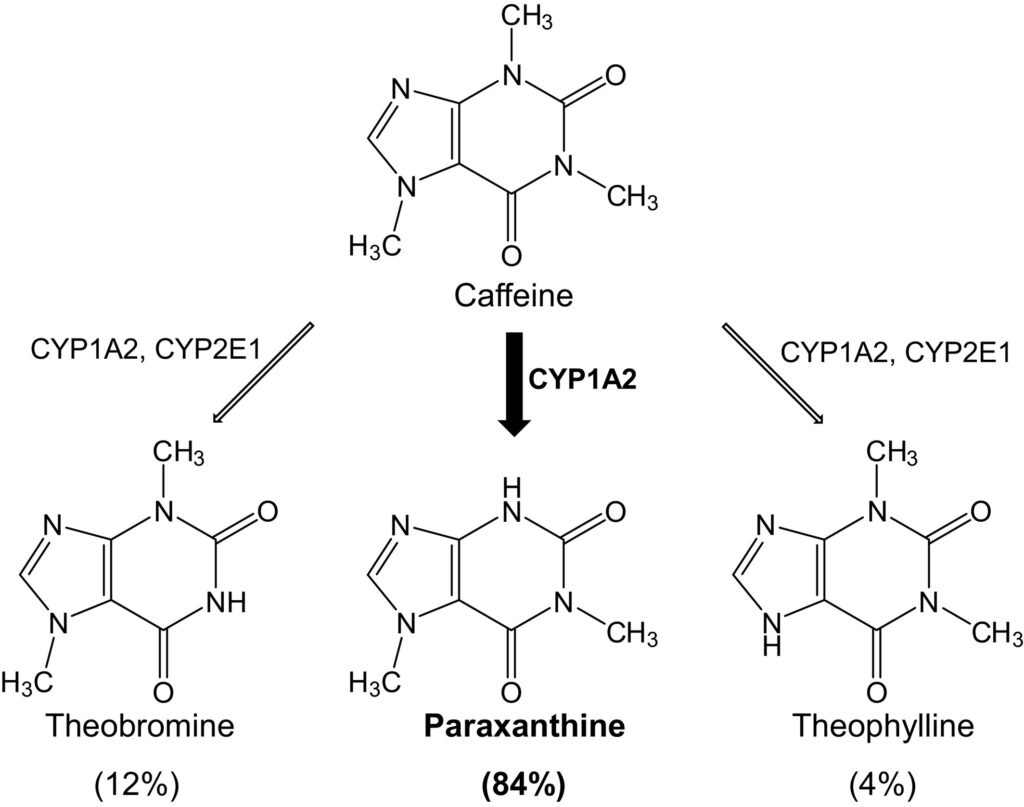
Intolleranza alla caffeina
Anche questa intolleranza ha un substrato genetico. Innanzitutto, la prima responsabile è la proteina che ha il compito di metabolizzare la caffeina: un citocromo P450 (CYP1A2). Questa proteina può essere un metabolizzatore ultra veloce, veloce (la normalità), lento. I metabolizzatori lenti hanno intolleranza alla caffeina.
Inoltre, altri due bersagli sono i due recettori dell’adenosina, ADORA1 e ADORA2A, che sono implicati in numerosi meccanismi biologici, tra cui la frequenza cardiaca e il sonno. Ancora una volta, per chi volesse approfondire, qui c’è una bella review.
Intolleranza alla miristicina
La miristicina è una sostanza contenuta nella noce moscata, il cui nome scientifico è Nux vomica (e già vi dovrebbe mettere in allarme). Anche la miristicina viene metabolizzata da un citocromo: in gran parte dal CYP3A4 e, in piccola parte, da CYP1A2 come la caffeina. Il discorso è analogo a quanto detto per la caffeina: ci sono metabolizzatori veloci e lenti, a secondo delle varianti di questo citocromo.
Intolleranza alla capsaicina
la capsaicina, invece, è contenuta nel peperoncino ed è quella che conferisce il sapore piccante e bruciante. Stavolta, la sensibilità alla capsaicina non dipende da un citocromo, ma proprio dalle varianti del recettore a cui si lega: TRPV1. Questo recettore è ubiquitario, su tutti gli epiteli, non solo quelli delle prime vie respiratorie, ma anche sulla pelle. Come sempre, per approfondire, trovate un articolo qui.
I test per diagnosticare le intolleranze sono affidabili?
Risposta molto semplice: no. Abbiamo visto che molto spesso di tratta di vere e proprie allergie per le quali esistono test validati scientificamente. Per quanto riguarda le intolleranze, buona parte sono su base genetica e quindi vanno evidenziate con un test genetico che trovi una mutazione causale nel gene. Per le intolleranze al lattosio, fruttosio e all’istamina posso essere eseguiti altri test non invasivi.
Per quanto riguarda i test che più vanno di moda, ossia il dosaggio delle IgG4, una particolare sottoclasse di immunoglobuline IgG, alla luce di quanto abbiamo detto, se fosse una reazione avversa ad un alimento mediata dal sistema immunitario non sarebbe più un’intolleranza, ma un’allergia. Ad oggi, non è mai stata dimostrata la correlazione tra IgG4 e intolleranze, anzi, sembrerebbe proprio che le IgG4 siano un segno di tolleranza del sistema immunitario e non viceversa. Concludendo, sembra essere unicamente una questione di marketing acchiappa soldi.












